nazwa przedmiotu: Filozofia
- tryb studiów - stacjonarne
- stopień studiów - I stopnia - inżynierskie
- kierunek studiów: Technologia chemiczna
- Nauczyciel: Przemysław Parszutowicz

nazwa przedmiotu: Filozofia
- tryb studiów - stacjonarne
- stopień studiów - I stopnia - inżynierskie
- kierunek studiów: Biotechnologia(WCh)
- Nauczyciel: Przemysław Parszutowicz
Kurs dotyczy zagadnień inżynierii materiałowej, elektrochemii, fizykochemii nanotechnologii materiałów stosowanych w budowaniu urządzeń elektrochemicznych do magazynowania i konwersji energii w urządzeniach. Prowadzony jest w języku angielskim.
- Nauczyciel: Anna Lisowska-Oleksiak
- Nauczyciel: Andrzej Nowak
Wykład przeznaczony dla studentów kierunku IBM II st.
Prowadzący prof. dr hab.inż. Anna Lisowska-OLeksiak
- Nauczyciel: Anna Lisowska-Oleksiak
- Nauczyciel: MARIUSZ Szkoda
- Nauczyciel: Zuzanna Zarach
Kierunek: Inżynieria Materiałowa (Studia II Stopnia - Semestr II)
Specjalność: Inżynieria Materiałów Polimerowych
Rok Akademicki: 2021/2022
WYKŁAD: prof. dr hab. inż. Janusz Datta - E-MAIL: janusz.datta@pg.edu.pl
LABORATORIUM: dr inż. Marcin Włoch - E-MAIL: marcin.wloch@pg.edu.pl
- Nauczyciel: Janusz Datta
- Nauczyciel: Ewa Głowińska
- Nauczyciel: PAULINA Kosmela
- Nauczyciel: PAULINA Parcheta-Szwindowska
- Nauczyciel: Łukasz Piszczyk
- Nauczyciel: Marcin Włoch
- Nauczyciel: Łukasz Zedler
Specjalność: Biotechnologia molekularna (WCh), II stopnia, stacjonarne
Prowadzący wykład: dr hab. Beata Krawczyk, prof. uczelni - forma stacjonarna
Prowadzący laboratoria: mgr inż. Bartosz Ostrowski - zajęcia stacjonarne na PG, sala 17 WCH C.
Kontakt: (58) 347-23-83
Beata Krawczyk (wykłady): e-mail: beata.krawczyk@pg.edu.pl; WCH B; p.218;
Bartosz Ostrowski, WCH B, p.218 tel. (58) 347-13-83
Konsultacje: stacjonarnie we wtorki po uprzednium umówieniu sie droga e-mailową. Konsultacje z laboratoriów do uzgodnienia z prowadzącym.
Opis kursu
Kurs dotyczy technik amplifikacji kwasów nukleinowych, zarówno tych związanych z amplifikacją matrycy, jak i tych stosowanych w amplifikacji sygnału czy sondy. Poza metodyką związaną z praktycznym stosowaniem różnych metod, omówione zostaną przykłady zastosowań różnych technik.
Laboratoria według planu zajęć
Zasady zaliczenia przedmiotu:
WYKŁAD
- obecność obowiązkowa (dozwolona 1 nieobecność na zajęciach), w przypadku dluższej nieobecności wymagane zwolnienie lekarskie
- zaliczenie wykładu w formie testu (stacjonarnie)
- próg zaliczenia dla wykładu - 60%
- wykład stanowi 50% składowej oceny końcowej
LABORATORIA
- obecność na laboratoriach jest obowiązkowa (jednanieobecność dozwolona)
- sprawozdania (forma do ustalenia z prowadzącym)
- próg zaliczenia dla laboratorium - 60%
- laboratoria stanowią 50% składowej oceny końcowej przedmiotu
Szczegółowy program
Wykłady: Dodatnie strony testów opartych o kwasy nukleinowe (NAT). Metody amplifikacji targetu. Organizacja laboratorium amplifikacji kwasów nukleinowych Historia techniki PCR. Zasada działania (pracy) PCR, kinetyka reakcji, pierwsze kroki w nastawianiu PCR, analiza produktów amplifikacji. Podstawy PCR – reagenty i urządzenia do PCR (termocyklery): matryce do PCR (kwasy nukleinowe), odczynniki (dNTP, Mg2+), bufory do PCR –skład, startery oligonukleotydowe, polimerazy do PCR (właściwości). Przygotowanie matrycy do PCR i inhibitory. Optymalizacja PCR. Rozwiązywanie problemów, substancje wpływające na efektywność PCR: inhibicja i wzmacnianie. HOT-start PCR. Touchdown PCR. Strony dodatnie stosowania PCR i ograniczenia (problemy z kontaminacją, zwalczanie i zapobieganie, kontrole w reakcji PCR). Poprawa specyficzności reakcji PCR. Wewnętrzny (zagnieżdżony) PCR (nested PCR) podnosi czułość reakcji. Złożony PCR (multiplex PCR). Asymetryczny PCR w przygotowywaniu ssDNA do sekwencjonowania. Analiza ekspresji genów w wykorzystaniem RT-PCR, semi-ilościowy i ilościowy PCR. Kompetytywny PCR. Allelo-specyficzna amplifikacja (ASA). Szybka amplifikacja końców cDNA (RACE). Metoda T-RFLP do badania mikroorganizmów środowiskowych. Podstawy Real-time PCR. Genotypowanie z zastosowaniem RAPD (przypadkowe amplifikowanie polimorficznego DNA). Metody oparte o ligację adaptorów oligonukleotydowych i PCR (LM PCR). Technika LAMP. Zróżnicowana liczba tandemowych powtórzeń w badaniach tożsamości. Zastosowanie PCR w diagnostyce molekularnej Alternatywne techniki amplifikacji kwasów nukleinowych (NASBA, TMA, SDA, MDA, OLA). Zastosowanie polimerazy Phi29. Metody amplifikacji sygnału (bDNA, hybryd capture assay) i metody amplifikacji sondy.
Laboratoria: Strategia optymalizacji reakcji PCR: optymalizacja temperatury przyłączania starterów, stężenia DNA - badanie czułości reakcji, optymalizacja dNTP i Mg2+, składu buforu do PCR. Badanie substancji wpływających na PCR: inhibitory i wzmacniacze. Inhibicja pochodząca od odczynników podczas izolacji DNA (proteinaza, fenol, SDS, EDTA, materiał biologiczny-krew). Efekt inhibicji określonego stężenia SDS na aktywność polimerazy i znoszenie działania hamującego SDS przez Tween20. Ocena efektywności działania wzmacniaczy (podnoszenie wydajności PCR z użyciem odpowiedniego panelu wzmacniaczy) Multiplex PCR - wykrywanie dwóch różnych regionów genomu w jednej probówce - optymalizacja.
- Nauczyciel: Beata Krawczyk
|
Nazwa przedmiotu: |
Diagnostyka Molekularna w Medycynie i Przemysle Spożywczym |
|
Kierunek studiów: |
Biotechnologia |
|
Wydział: |
Chemiczny |
|
Poziom kształcenia: |
Studia II Stopnia |
|
Forma studiów: |
Studia stacjonarne |
|
Rok studiów: |
II |
|
Semestr studiów: |
II |
|
Start semestru: |
październik 2021 |
|
Rok akademicki realizacji przedmiotu: |
2021/2022 |
|
Forma zajęć: |
blended learning Wykład - zdalny; Laboratoria - stacjonarnie |
Osoba odpowiedzialna za przedmiot: dr hab. Beata Krawczyk, prof. uczelni
Katedra Biotechnologii Molekularnej i Mikrobiologii PG (WCH B, pokój 218; e-mail: beata.krawczyk@pg.edu.pl)
Prowadzący: dr hab. Beata Krawczyk, prof. uczelni - wykład
Prowadzący: dr hab. inż. Anna Stanisławska-Sachadyn, prof. uczelni - laboratoria (e-mail: anna.stanislawska-sachadyn@pg.edu.pl); WCHC, pokój 101
Prowadzący: dr hab. inz. Roman Kotłowski, prof. uczelni - laboratoria (e-mail: roman.kotlowdski@pg.edu.pl); WCH B, pokój 218;
- Zajęcia z przedmiotu prowadzone będą w formie blended learning - wykłady w formie zdalnej jako e-nauczanie (15 godzin), laboratoria będą prowadzone metodą tradycyjną na uczelni (15 godzin).
- Wykłady rozpoczynają się 04.10.2021 r. w formie wideokonferencji (Webinarium), co poniedziałek, w godzinach 1015-1200 do 29.11.2021.
- Laboratoria będą odbywały się metodą tradycyjną w grupach według ustalonego planu zajęć w sali 17, WCh C. Dodatkowe informację (ogłoszenia, materiały uzupełniające) oraz Ouiz na platformie e- nauczanie.
Zasady zaliczenia e-kursu:
- Wykłady w formie zdalnej są obowiązkowe dla studenta, możliwa jest jedna nieobecność na wykładzie. Obecności będą zapisywane przez prowadzącego.
- Wykład kończy się quizem - warunkiem zaliczenia jest 60% poprawnych odpowiedzi.
- e-kurs stanowi 50% składowej oceny końcowej z przedmiotu
- zaliczenie laboratoriów - sprawozdania, quiz; próg zaliczenia laboratorium 60%, laboratorium stanowi 50% składowej oceny końcowej z przedmiotu
Elementy związane z komunikacją w ramach e-kursu:
- Konsultacje: możliwość komunikowania się w ramach e-kursu w formie zdalnej po skontaktowaniu sie drogą e-mailową z prowadzącym zajęcia w celu ustalenia terminu
- Dodatkowe informacje związane z wykładem będą przekazywane studentom w zakładce ogłoszenia oraz na forum e- nauczania
- Dodatkowy kontakt z prowadzącym e-kurs - konsultacje - piątek godzina 12; p. 218 CHB (stacjonarnie)
- Konsultacje z laboratoriów do uzgodnienia z osobą prowadzącą laboratoria.
Wymagania wstępne i dodatkowe:
Zaliczone przedmioty: Mikrobiologia, Biologia molekularna.
Dodatkowo: Immunologia ogólna
Cel przedmiotu
Celem przedmiotu jest zapoznanie studenta z metodami molekularnymi, stosowanymi w diagnostyce medycznej i przemyśle spożywczym, wykorzystanie osiągnięć i narzędzi biologii molekularnej w diagnostyce, pokazanie nowości na rynku diagnostycznym.
- Nauczyciel: Anna Brillowska-Dąbrowska
- Nauczyciel: Roman Kotłowski
- Nauczyciel: Beata Krawczyk
- Nauczyciel: Anna Stanisławska-Sachadyn
Specjalność: Biotechnologia molekularna (WCh), II stopnia, stacjonarne
Prowadzący wykład: dr hab. Beata Krawczyk, prof. uczelni - stacjonarnie na uczelni
Prowadzący laboratoria: mgr inż. Magdalena Fordon - zajęcia stacjonarne na PG, sala 17 WCH C.
Kontakt: (58) 347-23-83
Beata Krawczyk (wykłady): e-mail: beata.krawczyk@pg.edu.pl; WCH B; p.218;
Magdalena Fordon (laboratoria): magda.fordon@gmail.com; WCH B; p.218
Konsultacje: stacjonarnie w piątki o godzinie 12 - wykład; Konsultacje z laboratoriów - poniedziałek o godzinie 12.
Opis kursu
Kurs dotyczy technik amplifikacji kwasów nukleinowych, zarówno tych związanych z amplifikacją matrycy, jak i tych stosowanych w amplifikacji sygnału czy sondy. Poza metodyką związaną z praktycznym stosowaniem różnych metod, omówione zostaną przykłady zastosowań różnych technik.
Zasady zaliczenia przedmiotu:
WYKŁAD
- wykład w postaci webinariów, obecność obowiązkowa (dozwolona 1 nieobecność na zajęciach)
- zaliczenie wykładu w formie quizu
- próg zaliczenia dla wykładu - 60%
- wykład stanowi 50% składowej oceny końcowej
LABORATORIA
- obecność na laboratoriach jest obowiązkowa
- sprawozdania (forma do ustalenia z prowadzącym) oraz zadanie
- próg zaliczenia dla laboratorium - 60%
- laboratoria stanowią 50% składowej oceny końcowej przedmiotu
Szczegółowy program
Wykłady: Dodatnie strony testów opartych o kwasy nukleinowe (NAT). Metody amplifikacji targetu. Organizacja laboratorium amplifikacji kwasów nukleinowych Historia techniki PCR. Zasada działania (pracy) PCR, kinetyka reakcji, pierwsze kroki w nastawianiu PCR, analiza produktów amplifikacji. Podstawy PCR – reagenty i urządzenia do PCR (termocyklery): matryce do PCR (kwasy nukleinowe), odczynniki (dNTP, Mg2+), bufory do PCR –skład, startery oligonukleotydowe, polimerazy do PCR (właściwości). Przygotowanie matrycy do PCR i inhibitory. Optymalizacja PCR. Rozwiązywanie problemów, substancje wpływające na efektywność PCR: inhibicja i wzmacnianie. HOT-start PCR. Touchdown PCR. Strony dodatnie stosowania PCR i ograniczenia (problemy z kontaminacją, zwalczanie i zapobieganie, kontrole w reakcji PCR). Poprawa specyficzności reakcji PCR. Wewnętrzny (zagnieżdżony) PCR (nested PCR) podnosi czułość reakcji. Złożony PCR (multiplex PCR). Asymetryczny PCR w przygotowywaniu ssDNA do sekwencjonowania. Analiza ekspresji genów w wykorzystaniem RT-PCR, semi-ilościowy i ilościowy PCR. Kompetytywny PCR. Allelo-specyficzna amplifikacja (ASA). Szybka amplifikacja końców cDNA (RACE). Metoda T-RFLP do badania mikroorganizmów środowiskowych. Podstawy Real-time PCR. Genotypowanie z zastosowaniem RAPD (przypadkowe amplifikowanie polimorficznego DNA). Metody oparte o ligację adaptorów oligonukleotydowych i PCR (LM PCR). Technika LAMP. Zróżnicowana liczba tandemowych powtórzeń w badaniach tożsamości. Zastosowanie PCR w diagnostyce molekularnej Alternatywne techniki amplifikacji kwasów nukleinowych (NASBA, TMA, SDA, MDA, OLA). Zastosowanie polimerazy Phi29. Metody amplifikacji sygnału (bDNA, hybryd capture assay) i metody amplifikacji sondy.
Laboratoria: Strategia optymalizacji reakcji PCR: optymalizacja temperatury przyłączania starterów, stężenia DNA - badanie czułości reakcji, optymalizacja dNTP i Mg2+, składu buforu do PCR. Badanie substancji wpływających na PCR: inhibitory i wzmacniacze. Inhibicja pochodząca od odczynników podczas izolacji DNA (proteinaza, fenol, SDS, EDTA, materiał biologiczny-krew). Efekt inhibicji określonego stężenia SDS na aktywność polimerazy i znoszenie działania hamującego SDS przez Tween20. Ocena efektywności działania wzmacniaczy (podnoszenie wydajności PCR z użyciem odpowiedniego panelu wzmacniaczy) Multiplex PCR - wykrywanie dwóch różnych regionów genomu w jednej probówce - optymalizacja.
- Nauczyciel: MAGDALENA Burzyńska
- Nauczyciel: Beata Krawczyk
Wykład przeznaczony dla: Specjalność: Biotechnologia molekularna (WCh), I stopnia - inżynierskie, stacjonarne, Rok: 4, semestr: 7
Prowadzący:
dr hab. Beata Krawczyk, prof. uczelni (Bud. CHB, p.218); współprowadzenie mgr inż. Bartosz Ostrowski
Przedmiot jest prowadzony w formie stacjonarnej (s.27; CHA), laboratoria będą prowadzone metodą tradycyjną na PG (sala 17, WCH C).
kontakt z prowadzącym e-kurs: tel. 58 347-23-83; e-mail: beata.krawczyk@pg.edu.pl; konsultacje - piątek o godzinie 12, CHB (stacjonarnie), p.218;
Konsultacje w formie spotkania on-line - po uprzednim uzgodnieniu drogą e-mailową z prowadzącym zajęcia
Elementy komunikacyjne: forum, ogłoszenia na stronie e-nauczania, na danym przedmiocie oraz w trakcie zajęć laboratoryjnych, stacjonarnych
Zasady zaliczenia zajęć: próg zaliczenia dla przedmioty 60%;
Części składowe przedmiotu:
50% - wykład - próg zaliczenia 60% - w formie quizu na koniec wykładów; obecność na wykładach obowiązkowa (dozwolone 2 nieobecności)
50% - laboratoria - próg zaliczenia 60% - sprawozdania za 10 pkt każde (dozwolona 1 nieobecność)
- na e-kursie będą publikowane kolejne moduły tematyczne zawierające:
- wiedzę teoretyczną (prezentacje wykładów w formie PDF)
- odnośniki do materiałów pomocniczych odpowiadających wykładom i ćwiczeniom laboratoryjnym
- zadania do wykonania dla studentów - sprawozdania z określonym terminem oddania
- Studenci mają obowiązek regularnie zapoznawać się z materiałami dydaktycznymi oraz wykonać zamieszczone zadania oraz wziąć udział w webinariach.
- W połowie realizacji e-kursu oraz na jego zakończenie zostanie zamieszczona ankieta ewaluacyjna, którą należy wypełnić.
Tematyka wykładów:
Taksonomia i klasyfikacja mikroorganizmów
- Nomenklatura bakterii
- Klasyfikacja sztuczna i naturalna
Diagnostyka mikrobiologiczna oparta o cechy fenotypowe.
- Problemy wynikające ze stosowania metod fenotypowych w diagnostyce.
- Czy wszystkie drobnoustroje możemy hodować?
- Biofilmy jako zorganizowane społeczności bakterii.
Współczesna systematyka bakterii.
- Pojęcie gatunku bakteryjnego
- Metody badawcze – taksonomia molekularna
Ewolucja genomu bakteryjnego
- Z czego wynika zmienność ewolucyjna genomów?
- Rekombinacja genetyczna u podstaw ewolucji
Charakterystyka archeonów
- Przystosowanie archeonów do ekstremalnych warunków życia
Wzajemne stosunki między bakteriami, między bakteriami i bezkręgowcami, bakteriami i roślinami oraz między bakteriami i zwierzętami;
Patogeneza
- Mechanizmy ograniczające rozwój zakażenia;
- Rola toksyn w patogenezie.
- Budowa i mechanizm działania egzotoksyn i endotoksyn.
Komensalna mikrobiota człowieka.
Patogeny układu pokarmowego, wydalniczego i oddechowego.
Laboratorium: Pozyskiwanie czystych kultur bakteryjnych z hodowli mieszanych. Kolumna Winogradskiego; Bakteriologiczne badanie wody środowiskowej. Identyfikacja nieznanej bakterii - studia morfologiczne i charakterystyka fizjologiczna (testy utleniania i fermentacji, reakcje hydrolityczne, testy biochemiczna) Gram ujemne patogeny jelitowe - API 20E, testy tubowe); Paciorkowce - charakterystyka biochemiczna; Gronkowce - izolacja i identyfikacja.
- Nauczyciel: Anna Brillowska-Dąbrowska
- Nauczyciel: Beata Krawczyk
- Nauczyciel: BARTOSZ Ostrowski
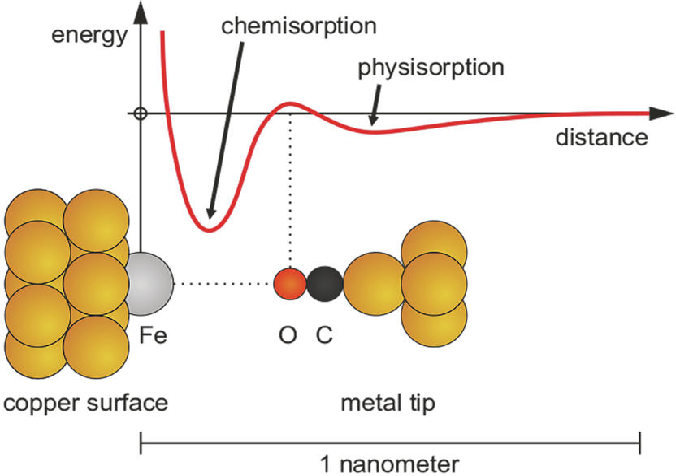
Kierunek - Chemia, semestr 5. Zadania, testy sprawdzające wiedzę, teoria dotycząca kinetyki reakcji chemicznych jak i zjawisk fizycznych towarzyszącym procesom katalitycznym.
- Nauczyciel: Joanna Krakowiak
Laboratorium z Chemii Organicznej,
Wybór preparatów, zaliczanie wejściówek, pokazy filmowe, komentarze do filmów, dyskusja, testy
- Nauczyciel: Klaudia Chmielewska
- Nauczyciel: MONIKA Gensicka-Kowalewska
- Nauczyciel: MAŁGORZATA Ryczkowska
Laboratorium z Chemii Organicznej,
Wybór preparatów, zaliczanie wejściówek, pokazy filmowe, komentarze do filmów, dyskusja, testy
- Nauczyciel: Klaudia Chmielewska
- Nauczyciel: MONIKA Gensicka-Kowalewska
Laboratorium z Chemii Organicznej,
Wybór preparatów, zaliczanie wejściówek, pokazy filmowe, komentarze do filmów, dyskusja, testy
- Nauczyciel: Klaudia Chmielewska
- Nauczyciel: MONIKA Gensicka-Kowalewska
Laboratorium z Chemii Organicznej,
Wybór preparatów, zaliczanie wejściówek, pokazy filmowe, komentarze do filmów, dyskusja, testy
- Nauczyciel: OLGA Ciupak
- Nauczyciel: MONIKA Gensicka-Kowalewska
Laboratorium z Chemii Organicznej,
Wybór preparatów, zaliczanie wejściówek, pokazy filmowe, komentarze do filmów, dyskusja, testy
- Nauczyciel: KAROL Biernacki
- Nauczyciel: MONIKA Gensicka-Kowalewska
- Nauczyciel: MICHAŁ Nowak
- Nauczyciel: NATALIA Jatkowska
- Nauczyciel: Błażej Kudłak
- Nauczyciel: Andrzej Nowak
- Nauczyciel: Ewa Wagner-Wysiecka

- Nauczyciel: BARTŁOMIEJ Cieślik
- Nauczyciel: Jan Mazerski
- Nauczyciel: Justyna Kucińska-Lipka