Wykład przeznaczony dla: Specjalność: Biotechnologia molekularna (WCh), I stopnia - inżynierskie, stacjonarne, Rok: 4, semestr: 7
Prowadzący:
dr hab. Beata Krawczyk, prof. uczelni (Bud. CHB, p.218); współprowadzenie mgr inż. Bartosz Ostrowski
Przedmiot jest prowadzony w formie stacjonarnej (s.27; CHA), laboratoria będą prowadzone metodą tradycyjną na PG (sala 17, WCH C).
kontakt z prowadzącym e-kurs: tel. 58 347-23-83; e-mail: beata.krawczyk@pg.edu.pl; konsultacje - piątek o godzinie 12, CHB (stacjonarnie), p.218;
Konsultacje w formie spotkania on-line - po uprzednim uzgodnieniu drogą e-mailową z prowadzącym zajęcia
Elementy komunikacyjne: forum, ogłoszenia na stronie e-nauczania, na danym przedmiocie oraz w trakcie zajęć laboratoryjnych, stacjonarnych
Zasady zaliczenia zajęć: próg zaliczenia dla przedmioty 60%;
Części składowe przedmiotu:
50% - wykład - próg zaliczenia 60% - w formie quizu na koniec wykładów; obecność na wykładach obowiązkowa (dozwolone 2 nieobecności)
50% - laboratoria - próg zaliczenia 60% - sprawozdania za 10 pkt każde (dozwolona 1 nieobecność)
- na e-kursie będą publikowane kolejne moduły tematyczne zawierające:
- wiedzę teoretyczną (prezentacje wykładów w formie PDF)
- odnośniki do materiałów pomocniczych odpowiadających wykładom i ćwiczeniom laboratoryjnym
- zadania do wykonania dla studentów - sprawozdania z określonym terminem oddania
- Studenci mają obowiązek regularnie zapoznawać się z materiałami dydaktycznymi oraz wykonać zamieszczone zadania oraz wziąć udział w webinariach.
- W połowie realizacji e-kursu oraz na jego zakończenie zostanie zamieszczona ankieta ewaluacyjna, którą należy wypełnić.
Tematyka wykładów:
Taksonomia i klasyfikacja mikroorganizmów
- Nomenklatura bakterii
- Klasyfikacja sztuczna i naturalna
Diagnostyka mikrobiologiczna oparta o cechy fenotypowe.
- Problemy wynikające ze stosowania metod fenotypowych w diagnostyce.
- Czy wszystkie drobnoustroje możemy hodować?
- Biofilmy jako zorganizowane społeczności bakterii.
Współczesna systematyka bakterii.
- Pojęcie gatunku bakteryjnego
- Metody badawcze – taksonomia molekularna
Ewolucja genomu bakteryjnego
- Z czego wynika zmienność ewolucyjna genomów?
- Rekombinacja genetyczna u podstaw ewolucji
Charakterystyka archeonów
- Przystosowanie archeonów do ekstremalnych warunków życia
Wzajemne stosunki między bakteriami, między bakteriami i bezkręgowcami, bakteriami i roślinami oraz między bakteriami i zwierzętami;
Patogeneza
- Mechanizmy ograniczające rozwój zakażenia;
- Rola toksyn w patogenezie.
- Budowa i mechanizm działania egzotoksyn i endotoksyn.
Komensalna mikrobiota człowieka.
Patogeny układu pokarmowego, wydalniczego i oddechowego.
Laboratorium: Pozyskiwanie czystych kultur bakteryjnych z hodowli mieszanych. Kolumna Winogradskiego; Bakteriologiczne badanie wody środowiskowej. Identyfikacja nieznanej bakterii - studia morfologiczne i charakterystyka fizjologiczna (testy utleniania i fermentacji, reakcje hydrolityczne, testy biochemiczna) Gram ujemne patogeny jelitowe - API 20E, testy tubowe); Paciorkowce - charakterystyka biochemiczna; Gronkowce - izolacja i identyfikacja.
- Nauczyciel: Anna Brillowska-Dąbrowska
- Nauczyciel: Beata Krawczyk
- Nauczyciel: BARTOSZ Ostrowski
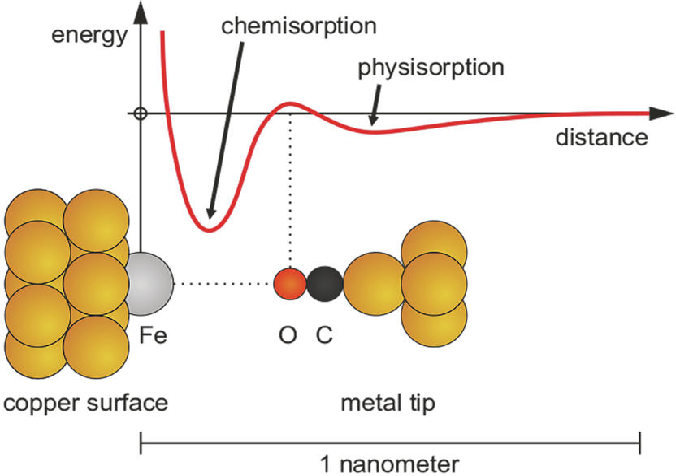
Kierunek - Chemia, semestr 5. Zadania, testy sprawdzające wiedzę, teoria dotycząca kinetyki reakcji chemicznych jak i zjawisk fizycznych towarzyszącym procesom katalitycznym.
- Nauczyciel: Joanna Krakowiak
Laboratorium z Chemii Organicznej,
Wybór preparatów, zaliczanie wejściówek, pokazy filmowe, komentarze do filmów, dyskusja, testy
- Nauczyciel: Klaudia Chmielewska
- Nauczyciel: MONIKA Gensicka-Kowalewska
- Nauczyciel: MAŁGORZATA Ryczkowska
Laboratorium z Chemii Organicznej,
Wybór preparatów, zaliczanie wejściówek, pokazy filmowe, komentarze do filmów, dyskusja, testy
- Nauczyciel: Klaudia Chmielewska
- Nauczyciel: MONIKA Gensicka-Kowalewska
Laboratorium z Chemii Organicznej,
Wybór preparatów, zaliczanie wejściówek, pokazy filmowe, komentarze do filmów, dyskusja, testy
- Nauczyciel: Klaudia Chmielewska
- Nauczyciel: MONIKA Gensicka-Kowalewska
Laboratorium z Chemii Organicznej,
Wybór preparatów, zaliczanie wejściówek, pokazy filmowe, komentarze do filmów, dyskusja, testy
- Nauczyciel: OLGA Ciupak
- Nauczyciel: MONIKA Gensicka-Kowalewska
Laboratorium z Chemii Organicznej,
Wybór preparatów, zaliczanie wejściówek, pokazy filmowe, komentarze do filmów, dyskusja, testy
- Nauczyciel: KAROL Biernacki
- Nauczyciel: MONIKA Gensicka-Kowalewska
- Nauczyciel: MICHAŁ Nowak
- Nauczyciel: NATALIA Jatkowska
- Nauczyciel: Błażej Kudłak
- Nauczyciel: Andrzej Nowak
- Nauczyciel: Ewa Wagner-Wysiecka

- Nauczyciel: BARTŁOMIEJ Cieślik
- Nauczyciel: Jan Mazerski
- Nauczyciel: Justyna Kucińska-Lipka
- Nauczyciel: Jan Mazerski
Dla kierunku Korozja na II stopniu studiów (2 semestr)
- Nauczyciel: Joanna Krakowiak
Microbiology interactive lectures are dedicated to those who are interested in the role of microorganisms on our planet and their interaction with other living organisms and inorganic elements as well as more complex chemical compounds.
- Nauczyciel: Roman Kotłowski
Tematyka kursu porusza podstawową terminologię angielska z zakresu chemii i technologii chemicznej (zagadnienia związane z wybraną aparaturą laboratoryjną i technologiczną, budową związków chemicznych, procesami technologicznymi i innymi zagadnieniami z zakresu danej specjalizacji). Kurs na studentów kierunku: Technologia Chemiczna, semestr VI, grupa zajęciowa TPKiMF (sem 2020/2021).
- Nauczyciel: Anna Brillowska-Dąbrowska
- Nauczyciel: Agnieszka Głowacz-Różyńska
- Nauczyciel: Ewa Głowińska
- Nauczyciel: Ilona Kłosowska-Chomiczewska
- Nauczyciel: Adam Macierzanka
- Nauczyciel: Andrzej Nowak
Wykład
- Nauczyciel: Zofia Mazerska
Kierunek - Technologie Ochrony Środowiska, semestr III. Na kursie przedstawiane będą definicje podstawowych pojęć, wzory z termodynamiki, kinetyki i równowag fazowych. Przygotowane będą zadania i pytania na różnym stopniu trudności.